化学が得意になるにはまず特定の物質の基礎的な情報を理解しておく必要があります。
中でも代表的な化学物質として「炭素」がありますが「意外と覚えにくい物質」といえるでしょう。
ここでは、この炭素に着目して「炭素の原子番号・質量数・原子量・陽子数・中性子の数・価電子数(最外殻電子数)・原子価は?」について解説していきますので、参考にしてみてください。
炭素の原子量・質量数は?
それではまず炭素の原子量・質量数を見ていきましょう。
結論からいいますと
・炭素の原子量は約12
・炭素の質量数はほとんどが12(ごく一部に同位体の11,13,14などあり)
です。

原子量は各々の質量数の炭素に割合をかけたものを足し合わせた数であり、重みづけを考慮した平均値のようなものといえます。
原子量と質量数は炭素だけでなく、上のような意味の違いがあるので注意して覚えておきましょう。
炭素の原子番号・陽子数・中性子の数は?
今度は炭素の原子番号・陽子数・中性子の数についても見ていきます。
結論からいいますと
・炭素の原子番号は6
・炭素の陽子数も6
・炭素の中性子数はほとんどは6(ごく一部で5,7,8)
です。

まず炭素の原子番号はあくまで定義のため覚えておきましょう。なお、原子番号は陽子数のことを指すと決められているため、炭素の陽子数はこちらも6で同じとなります。
一方で中性子数とは、中性子数=質量数―陽子数で計算できる数値のため、炭素には同位体があり各々の質量数が11,12,13,14とあることから、中性子数も5,6,7,8,という値をとるのです。
ただ、炭素はほとんどが質量数12、中性子数6という化学構造になっていると覚えておきましょう。
炭素の価電子数(最外殻電子数)・原子価は?【結合の手】
続いて、結合に関係する指標である炭素の価電子数(最外殻電子数)・原子価について解説していきます。
結論からいいますと
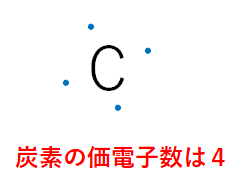
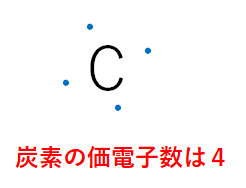
・炭素の価電子数(最外殻電子数)は4
です。
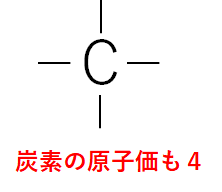
・炭素の原子価も4です。
まず炭素の価電子数(最外殻電子数)とは、炭素が持つ結合に関係する最外殻の電子の数のことであり、4つ分の電子があることになります。
一方で、原子価とは「結合の手」を意味し、炭素の場合では電子4つがすべて不対電子となるため、結合の手も4本となるわけですね。
関連記事として
・炭素の化学式(元素記号)やイオン式や燃焼の反応式などについてはこちら
で解説のため、併せてチェックしてみてください♪
まとめ 炭素の質量数・原子量・陽子数・中性子の数・原子番号は?
ここでは、炭素の価電子数(最外殻電子数)・原子価・原子番号・質量数・原子量・陽子数・中性子の数は?について解説しました。
炭素の価電子数(最外殻電子数)・原子価・原子番号・質量数・原子量・陽子数・中性子の数は覚えにくいため、この機会に理解しておくといいです。
炭素を始めとしたさまざまな物質の知識を身に着け、もっと化学を楽しんでいきましょう。