化学が得意になるにはまず特定の物質の基礎的な情報を理解しておく必要があります。
中でも代表的な化学物質として「硫化水素」がありますが「意外と覚えにくい物質」といえるでしょう。
ここでは、この硫化水素に着目して「化学式・分子式・電子式・構造式・分子量・極性や分子の形(折れ線か直線か)?」などについて解説していきますので、参考にしてみてください。
硫化水素の化学式・分子式はSO2
それではまず、硫化水素の化学式・分子式について確認していきましょう。
結論からいいますと硫化水素の化学式(分子式)は「H2S」と表現されます。
※
H2Sの
化学式の後ろから
・S:硫化
・H2:水素
となると覚えておきましょう。
なお、硫化水素の組成式も同じH2Sとなります。
硫化水素の分子量・式量は?
今度は硫化水素の分子量・式量についても見ていきましょう。
結論からいいますと、硫化水素の分子量・式量は34です。
※
これは上の硫化水素の化学式・分子式から導出することができ、S:32、H:1を元に「(1×2) + 32 = 34 」となります。
硫化水素の電子式や構造式は?
硫化水素の電子式・構造式も見ていきましょう。
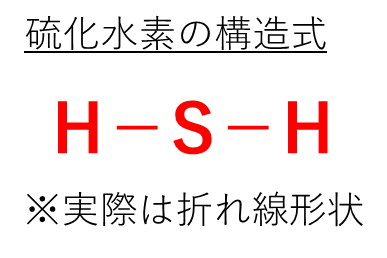
硫化水素の構造式は以下の通り。共有結合でS-Hが結びついています。
なお、実際は折れ線型の分子構造のため、注意して覚えましょう。
硫化水素の電子式は以下の通りです。

同様に硫黄Sを含む化合物の二酸化硫黄の構造式・電子式よりも簡単に理解できますね。
硫化水素の分子の形や極性は?なぜ?
硫化水素の分子構造は「折れ線型」です。
上述の硫化水素の電子式からもわかるよう、Sは8個の電子対を持っています。
2個ずつの4組の電子対となる際、各々の電子対はマイナスの電荷を帯びているため、お互いが反発し、離れたところが安定した位置になるのです。そのため、Sを中心として四面体構造を取るのがイメージできるでしょう。
そのうちの2つにH元素がつくために、折れ線型となります。
これが、硫化水素の分子の形が直線でなく、折れ線形状となる理由です。
このような分子の形のため、硫化水素は極性分子となります。
さらに、SとHには電気陰性度の差がある(Sの方がHよりも大きく、電荷がマイナスに偏っている)ことからも、極性があることがわかりますね。
関連物質の
・硫黄の化学式・元素記号などの詳細はこちら
で解説していますので、併せてチェックしてみてください。
まとめ 硫化水素の電子式・構造式・分子量・極性や分子の形は?
ここでは硫化水素の化学式・分子式・電子式・構造式・分子量・極性や分子の形は?について解説しました。
硫化水素の各情報は覚えにくいため、この機会に理解しておくといいです。
硫化水素を始めとしたさまざまな物質の知識を身に着け、もっと化学を楽しんでいきましょう。